Ausgansmaterial Kollagen
Die Bildung des (unlöslichen) Bindegewebskollagens
kann in drei Stufen unterteilt werden. Zuerst erfolgt nach der Bildung des
sogenannten Tropokollagen-Moleküls in der Zelle und dessen Abgabe in
den intrazellulären Raum der Übergang vom neutralsalzlöslichen
Tropokollagen über das noch säurelösliche Prokollagen zum durch
weiteres Altern unlöslichen Bindegewebs-Kollagen.
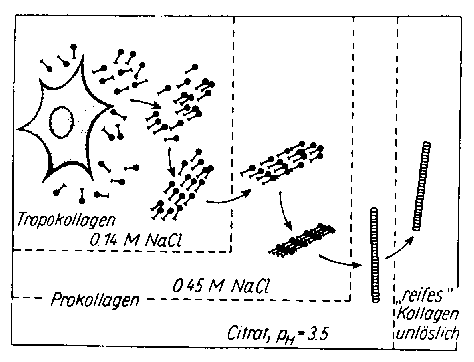
Zur Gelatinegewinnung wird nun das unlösliche
Kollagen soweit hydrolysiert, dass es wieder in einer wasserlöslichen
Form mit optimalen physikalischen Eigenschaften vorliegt.
Vorbehandlung
Die Rostoffe zur Herstellung von Gelatine kommen bei rennomierten Herstellern ausschliesslich aus Schlachthäusern, die zertifiziert und veterinärärztlich überwacht sind. So ist sichergestellt, daß nur zum menschlichen Verzehr geeignetes Material eigesetzt wird. Nach intensiver Reinigung des Rohmaterials werden je nach Rohstoff unterschiedliche Verfahren angewandt, um das zunächst wasserunlösliche (Binde)Gewebe so zu lockern (durch Aufbrechen von Bindungen), dass es in heißem Wasser löslich wird.
Zwei Aufschlußverfahren werden bei der Herstellung
von Gelatine unterschieden:
Alkalisches Aufschlußverfahren (ergibt Gelatine vom Typ B):
Die Gewebsstruktur von (Rinder)Knochen (sowie
Rinderspalt - Unterhaut des Rindes-) lässt sich nur durch längere
Behandlung mit Kalkmilch schonend aufschließen (wasserlöslich
machen).
Mazeration der Knochen
Die Knochen müssen zunächst aber von ihren mineralischen Bestandteilen befreit werden. Durch Einwirkung einer Säure - im allgemeinen Salzsäure - werden die sonst unlöslichen Calciumphosphate und -carbonate herausgelöst. Der Prozess, auch Mazeration genannt, wird dabei so geführt, dass der organische Teil des Knochens, das Ossein, nicht angegriffen wird. Als Reaktionsgefäße dienen immer noch große Holzkessel, da diese weniger von den Säuren angegriffen werden. Die Mazerierungstemperatur soll nicht über 25°C steigen. Die Mazeration verläuft exotherm und lässt sich durch folgende Reaktionsgleichungen systematisch darstellen:
Ca3 (P04)2 +
4 HCl ---> Ca(H2P04)2
+ 2 CaCl2 + Q
(Mg, Ca)CO3 + 2 HCl ---> Mg,
CaCl2 + H20 + CO2 + Q
Tricalciumphosphat geht in Lösung unter Bildung von Calciumdihydrogenphosphat. Nach Beendigung der Mazerierung ist das Ossein glasig gequollen, es ist elastisch und hat noch die ursprüngliche Form des Knochens. Wichtig ist beim Aufschluss die Säurekonzentration. Am günstigsten ist eine Salzsäure mit 5 bis 6° Bé, deren Dichte während der Mazeration nicht über 13° Bé durch die Aufnahme von Phosphorsäure und Calciumdihydrogenphosphat ansteigen soll. Es könnte sonst eine Verfestigung des gesamten Knochenmaterials, auch Betonierung genannt, eintreten. Das gelöste Calciumdihydrogenphosphat reagiert dabei wieder mit dem noch ungelösten Calciumphosphat zu Calciumhydrogenphosphat, das sich niederschlägt und die Knochen miteinander verkittet (betoniert):
Ca(H2PO4)2 + Ca3(P04)2 ---> 4 CaHP04 Ca(H2PO4)2 +
CaCO ---> 4 CaHP04
+ 3 H2O + CO2
Das kalkalkalische Verfahren
Häute bzw. das wie oben beschrieben erhaltene
Ossein wird beim klassische kalkalkalische Zweistufen-Verfahren in der ersten
Stufe durch Zusatz von Kalkmilch einem mehrwöchigem Äscherungsprozess
unterworfen. Dabei werden sowohl sequentielle Peptidbindungen als auch Quervernetzungen
zwischen den einzelnen Polypeptidketten partiell aufgespalten. An den Quervernetzungen
sind Esterbindungen beteiligt, außerdem werden auch amidartige Querverbindungen,
an denen ε-Amino- und auch δ-Guanidinogruppen beteiligt sind, angenommen.
Der größte Teil davon ist zwischen den einzelnen Tropokollagen-Molekülen
anzutreffen, der Rest als intramolekulare Brückenglieder zwischen den
Tropokollagen-Untereinheiten. Auch die meisten Säureamidgruppen der
Glutamin- und Asparaginsäure werden unter Ammoniak-Abspaltung verseift.
Die Äscherzeit dauert durchschnittlich zwei bis drei Monate, wobei die
Kalkmilch meist zwei- bis dreimal erneuert wird. Zur Fabrikation einer einwandfreien
Photoemulsionsgelatine ist ein mehrmaliges Erneuern unerlässlich.
Zusammensetzung der Knochen (Durchschnittswerte).
Mineralische Bestandteile:
| löslich in H2O | 1,25 % |
| unlöslich in heißem H2O | 69,66 % |
Diese 70,91 % mineralische Bestandteile setzen sich zusammen aus:
| Calciumphosphat | 85,0 % |
| Calciumcarbonat | 10,0 % |
| Magnesiumphosphat | 1,5 % |
| Calciumfluorid | 0,3 % |
| Calciumchlorid | 0,2 % |
| Alkalisalze | 2,0 % |
| Kollagengehalt (Ossein) | 18,64 % |
| Mucopolysaccarid | 0,24 % |
| Eiweißstoffe, beständig gegen heißes H2O | 1,02 % |
| Wasser (Gewichtsverlust bei 105o C) | 8,18 % |
Die Äscherungstemperatur wird im allgemeinen
zwischen 5 und 15° C gehalten. Jedoch stellt sich die Hydrolysenintensität
durch eine spezielle Eigenschaft des Kalkes von selbst ein. Die geringe Löslichkeit
des Kalkes nimmt mit der Temperaturerhöhung noch weiter ab, z.B. löst
1 Liter Wasser bei O° C 1,31 g CaO, bei 20° C 1,203 g CaO. Damit
tritt eine Art Selbsteinstellung des Gehaltes an gelöstem Kalk ein,
welche teilweise die Vergrößerung der Kollagenhydrolyse mit der
Temperatur kompensiert. Die Sudreife wird in der Praxis im allgemeinen durch
standardisierte Probeverkochungen ermittelt. Ein Hautmaterial oder das Ossein
ist dann ausreichend geäschert, wenn es bei 60°C, einem Sud-ph 6
und einer Extraktionsdauer von fünf Stunden eine Gelatineausbeute von
rd. 75 % ergibt. Zur Ermittlung der Sudreife können ebenso die Bestimmung
des Gesamt- wie auch die des Amidstickstoffs herangezogen werden. Der Gesamtstickstoff
nimmt mit zunehmender Äscherdauer ab und vermindert sich um 1 bis 2
%. absolut. Der Amidstickstoff verringert sich von 0,4 bis 0,5 % auf 0,12
bis 0,14 %. Th. Altenschöpfer konnte ermitteln, dass der Endwert der
Verkochbarkeit (75 % Gelatineausbeute) mit dem Zeitpunkt des für die
Sudreife kennzeichnenden Amid-N-Wertes (0,12-0,14 %) zusammenfällt.
Nach Beendigung des Äscherns wird das Material
gewaschen, zur Beseitigung des restlichen Kalkes angesäuert, säurefrei
gewaschen und auf den gewünschte Sud-pH eingestellt. Danach beginnt
die zweite Stufe des kalkalkalischen Aufbereitungsverfahrens. Durch Verkochen
in einer leicht angesäuerten wässerigen Lösung bei 60°C
setzt die Lösungshydrolyse ein. Auf diese Weise wird die thermische
Eiweißdenaturierung eingeleitet, die das Wasserstoffbindungssystem
als wichtigsten Stabilisierungsfaktor der Kollagenstruktur aufhebt. Die Lösungshydrolyse
soll möglichst milde durchgeführt werden, so dass ein weiterer
Abbau der Peptidbruchstücke vermieden wird.
Saures Aufschlussverfahren (ergibt Gelatine vom Typ A):
Die Rohstoffe (Schweineschwarten, Schweineknochen, Geflügelknochen, Rinderknochen) werden bei diesem Verfahren einige Tage mit Säure behandelt (z.B. Schwefelsäure), wobei diese mehrmals erneuert wird, und anschließend die Gelatine mit heißem bis siedendem Wasser extrahiert.
Das einstufige saure Verfahren das dem zweiten Schritt im kalkalkalischen Prozess entspricht wird vorwiegend zum Aufschluss des Schweineschwartenkollagens eingesetzt. Dies hängt damit zusammen, dass die Leichtigkeit, mit der aus einem Kollagen-Gewebe die Gelatine extrahiert werden kann, weitgehend mit der Art und dem Alter des Tieres variiert. Aus den Schwarten lässt sich Gelatine allein auf Grund ihres relativ geringen Alters leichter gewinnen als aus z.B. Rinderhäuten.
Das Verkochen des vorbehandelten Kollagens ist
eine diskontinuierliche Stufenextraktion. Es wird bei einer Temperatur von
60°C begonnen, die allmählich von Extraktionsstufe zu Extraktionsstufe
(Boullions genannt) auf 90 bis 95°C erhöht wird. Je nach Gelatinequalität
wird das Versieden bei einer Gelatinekonzentration von 3½ bis 6 %
unterbrochen und die Lösung abgezogen. Auf diese Weise werden im allgemeinen
vier bis fünf Abzüge durchgeführt.
Vorgänge beim Aufschluss des Kollagens
Die Säureeinwirkung leitet die topochemische Hydrolyse ein, die durch Erwärmung des Materials gesteigert wird. Mit der Erwärmung setzt die thermische Eiweißdenaturierung ein, deren Folge der starke Abbau des Kollagens zu Gelatine ist. Die Vorzüge dieses Aufschlussprozesses ist seine Kürze. Er erspart die langwierige Äscherung und damit Betriebskapital und liefert Gelatine mit sehr hoher Gallertfestigkeit und Viskosität (Bloomzahl bis zu 300 als erstarrte 6 2/3 %ige Lösung bei 10°C - Viskosität bis zu 150 mP, gemessen in 6 2/3%iger Lösung bei 60°C). Allerdings ist das pH-Intervall sehr eng begrenzt, in dem Gelatinequalitäten mit extrem guten physikalischen Daten erhalten werden. Zusammenfassend kann die Überführung des Kollagens in Gelatine in drei Reaktionen unterteilt werden.
1. K e t t e n v e r k ü r z u n g durch Spaltung von Peptidbindungen,
2. S p a l t u n g hauptvalenzmäßiger Quervernetzungen,
3. A u f l ö s u n g der Schraubenstruktur
des Kollagens.
Die beiden ersten Reaktionen erfährt das Kollagen bei der Vorbehandlung sowohl durch Äscherung als auch durch Säureeinwirkung. Sie unterscheiden sich aber in ihrer Geschwindigkeit. Bei Säureeinwirkung laufen die Vorgänge 1 und 2 gleich schnell ab, bei einer Kalkbehandlung dagegen werden im Verhältnis mehr Quervernetzungen als Peptidbindungen gespalten. An Hand von systematischen Untersuchungen konnte nachgewiesen werden, dass bei vorangegangener Kalkäscherung 17mal mehr Querverbindungen als in der Sequenz stehende Peptidbindungen gelöst werden.
Der Vorgang 3 erfolgt bei der Exraktion mit warmen
Wasser, d.h. bei der thermischen Denaturierung, eigentlichen Verkochen. Nach
Befunden kann gefolgert werden, dass eine kalkalkalisch aufgeschlossene Gelatine
vorwiegend aus verknäuelten, einsträngigen Peptidketten besteht,
zwischen denen - anders als bei sauer vorbehandelter Gelatine - die meisten
Quervernetzungen gelöst sind. Bei einer sauer aufgearbeiteten Gelatine
werden auf Grund ihres physikalischen Verhaltens seitlich verknüpfte
Aggregate von Peptidbruchstücken angenommen, die dem Tropokollagen noch
bis zu einem gewissen Grad nahestehen.
Reinigung
Die bei der Extraktion gewonnene Gelatinelösung
wird anschließend von Fett und Schwebeteilchen befreit. Dies geschieht
einerseits mit Seperatoren und adererseits mit Filtern, in denen Verunreinigungen
zurückgehalten werden. Ionenaustauscher (Säulen, die mit Austauschharzen
gefüllt sind) bilden die nächste Reinigungsstufe. Wie bei der Wasserenthärtung
dienen diese bei Gelatine dazu, je nach Anforderung mehr oder weniger vollständig
Calcium, Natrium, Säureresten und anderen Salzen zu entfernen.
Konzentrierung
Vakuum-Eindampfanlagen konzentrieren die Gelatinelösung
schonend bis zu einer dickflüssigen, honigartigen Beschaffenheit. Diese
hochviskosen Lösungen werden nochmals durch Filter geleitet, um die
letzten Schwebeteilchen zu entfernen. Die hochkonzentrierten Gelatinelösungen
werden anschliessend in einer Kurzzeit-Hocherhitzungsanlage (UHT) einer Sterilisation
unterworfen, abgekühlt und dann gelieren lassen.
Trocknen
Der so erhaltene Gelatinegelee wird durch ein
Lochsieb extrudiert und die dabei enstehenden "Gelee-Nudeln" gleichmäßig
auf das Band eines Trockners verteilt. In diesem wird mit konditionierter
(gefilterte, gewaschene, vorgetrocknete und entkeimte) Luft die Gelatine getrocknet.
Am Ende des Trockners (bis 50 m lange Röhre) werden die auf 10-12% Wassergehalt
heruntergetrockneten Gelatine-Nudeln gebrochen und gemahlen und dann im Zwischenlager
bis zur weiteren Verwendung gelagert. Die einzelnen Chargen (Extraktionen)
von jeweils bis zu 2.000 kg werden im Labor physikalische, chemisch und bakteriologisch
geprüft und aufgrund dieser Analysen freigegeben bzw. bei Spezifikationsabweichung
gegebenfalls auch gesperrt.
Mahlen, Sieben, Mischen
Um eine bestimmte Qualität zu erzielen bzw.
auch größere Chargen zu bekommen, müssen meist mehrere Extraktionen
gemischt werden. Anhand der Analysewerte errechnet dabei ein Computerprogramm
die Anteile der einzelnen Extraktionen, die zusammengemischt werden müssen,
um die vom Kunden gewünschte Kennzahlen/Qualität für diese
Gelatinecharge zu erzielen. Um spezifischen Kundenanforderungen zu entsprechen,
wird Gelatine in unterschiedlichen Korngrößen hergestellt, Hierzu
werden je nach der gewünschten Korngöße unterschiedliche
Mühlen eingesetzt bzw. auch Sieb/Windsicht-Einrichtungen, um den durch
die Mahlung enstandenen, unerwünschten Feinanteil zu entfernen.
Gelatinestruktur und -eigenschaften
wichtige Kennzahlen von Gelatine
Gelierkraftverlust durch pH/Temperatur
Arzneibuchspezifikationen
Literaturübersicht (bis 1980)
Hydrokolloide in Milcherzeugnissen
Koazervation mit Gelatine


